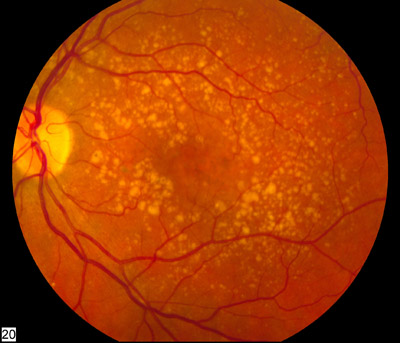
La dégénérescence maculaire liée à l'âge (DMLA) est une maladie chronique et évolutive de la macula, la zone centrale de la rétine responsable de la vision fine, détaillée et des couleurs. La macula concentre les photorécepteurs de type cônes, spécialisés dans la perception des couleurs, des contrastes et des détails fins. C'est cette région qui nous permet de lire, de reconnaître les visages et de conduire. La DMLA touche les sujets de plus de 50 ans et concerne plus d'un million de personnes en France, constituant la première cause de cécité légale dans les pays industrialisés.
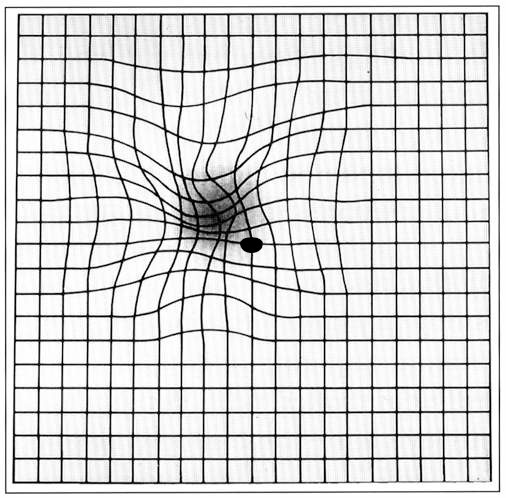
La prévalence augmente fortement avec l'âge : environ 1 % à 55 ans, 10 % à 70 ans et jusqu'à 25-30 % au-delà de 80 ans. La DMLA se traduit par une perte progressive de la vision centrale : difficulté à percevoir les couleurs, les contrastes et les détails, apparition d'une tache au centre du champ visuel (scotome), et déformation des images dans le champ de vision central (métamorphopsies). La vision périphérique est préservée, mais la vision centrale, la plus utile au quotidien, se dégrade progressivement ou brutalement selon la forme.