Les tumeurs oculaires regroupent un ensemble de lésions bénignes et malignes pouvant toucher l'ensemble des structures de l'œil et de ses annexes. Elles se répartissent en tumeurs intraoculaires (choroïde, rétine, iris, corps ciliaire), tumeurs orbitaires (tissus entourant le globe) et tumeurs annexielles (paupières, conjonctive, voies lacrymales). La diversité de ces lésions impose une démarche diagnostique rigoureuse, associant examen clinique spécialisé et imagerie multimodale.
Le diagnostic précoce est un enjeu majeur en oncologie oculaire. Pour les tumeurs malignes comme le mélanome uvéal, la détection à un stade précoce permet non seulement de préserver la vision et le globe oculaire, mais aussi d'améliorer considérablement le pronostic vital. En effet, le mélanome uvéal présente un risque de dissémination métastatique, principalement hépatique, dont la probabilité augmente avec la taille tumorale au moment du diagnostic.
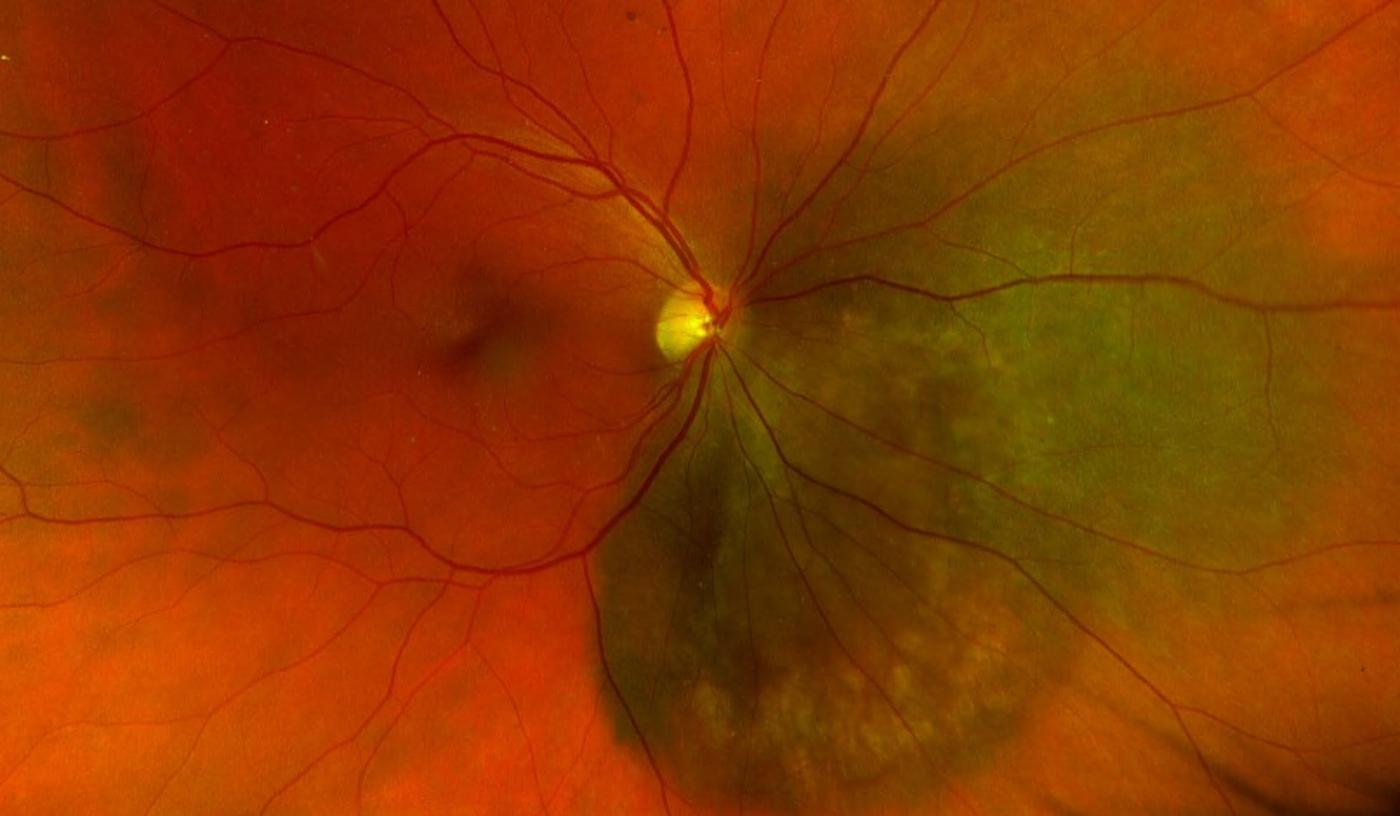
À l'Institut Parisien d'Ophtalmologie, nous disposons d'un plateau technique complet pour le dépistage et la caractérisation des tumeurs oculaires : rétinophotographie grand champ OPTOS, OCT haute résolution, échographie oculaire en mode B et autofluorescence. Cette approche multimodale permet de poser un diagnostic précis et d'orienter rapidement les patients vers les centres de référence en oncologie oculaire pour la prise en charge thérapeutique.