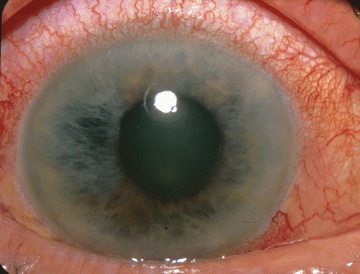
Le glaucome est une neuropathie optique chronique et progressive, le plus souvent liée à une élévation de la pression intraoculaire (PIO). Surnommé le « voleur silencieux de la vue », il détruit progressivement les fibres nerveuses rétiniennes qui transmettent les images au cerveau, sans douleur ni symptôme apparent pendant des années.
En France, plus d'un million de personnes sont touchées, et près de la moitié l'ignorent. Dans le monde, le glaucome est la deuxième cause de cécité après la cataracte, avec environ 80 millions de personnes atteintes et plus de 10 millions de cas de cécité bilatérale. L'Organisation Mondiale de la Santé estime que ce chiffre atteindra 112 millions en 2040, en raison du vieillissement de la population mondiale.
En Europe, la prévalence du glaucome à angle ouvert est estimée à 2,4 % chez les plus de 40 ans, atteignant 7 % au-delà de 80 ans. Le coût socio-économique est considérable : perte d'autonomie, chutes, accidents de la route et détérioration de la qualité de vie. Sans prise en charge, il entraîne une perte irréversible du champ visuel, pouvant mener à la cécité complète.