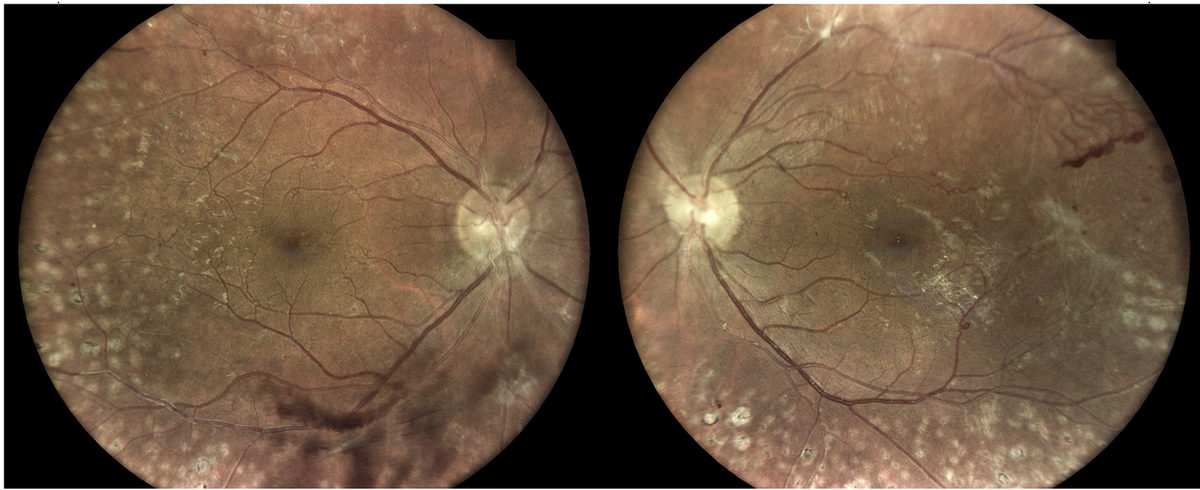
La rétinopathie diabétique (RD) est une complication microvasculaire du diabète (type 1 et type 2) qui atteint les petits vaisseaux de la rétine. Elle représente la première cause de cécité avant 50 ans dans les pays industrialisés et la principale cause de malvoyance chez les adultes en âge de travailler.
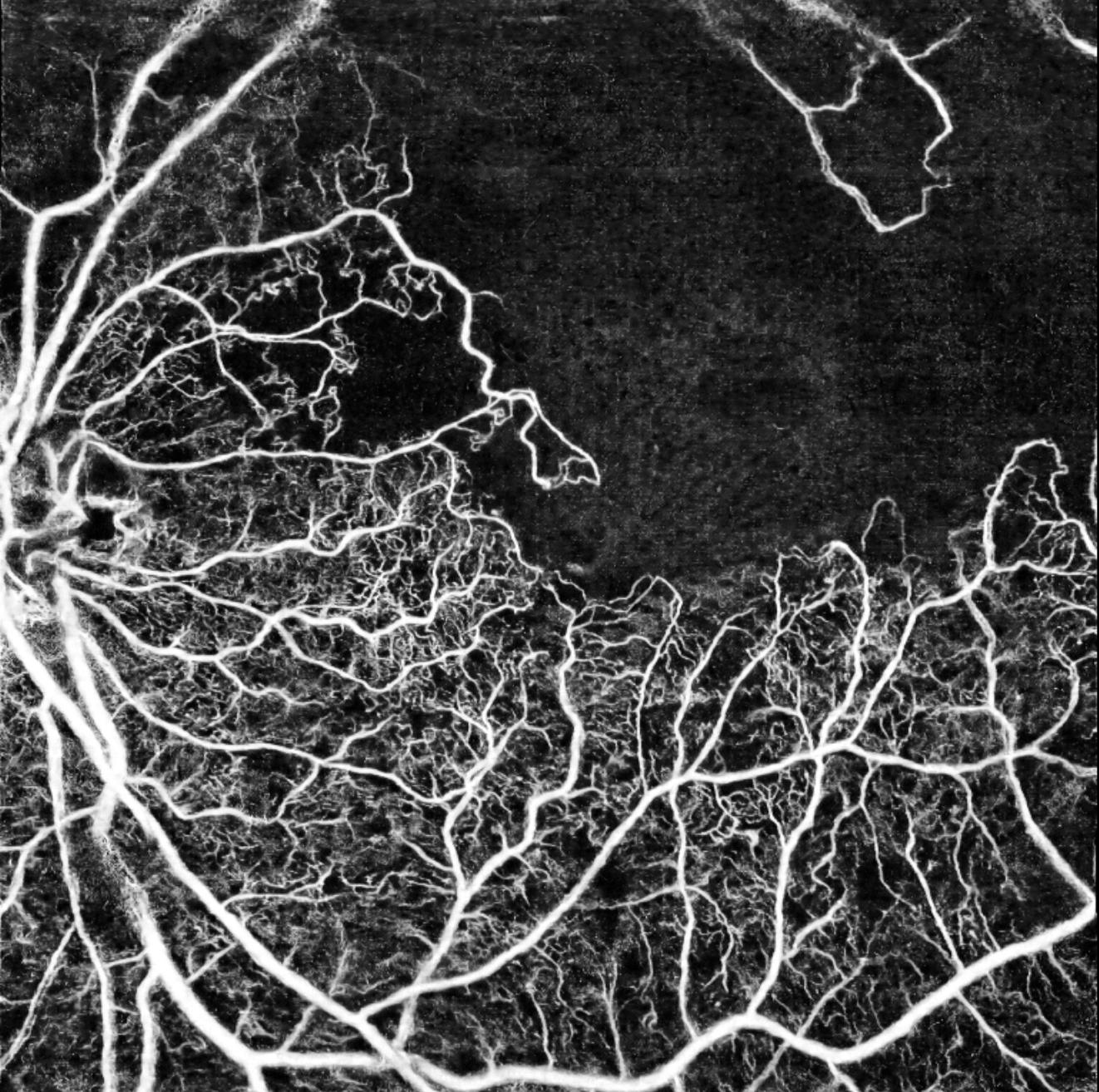
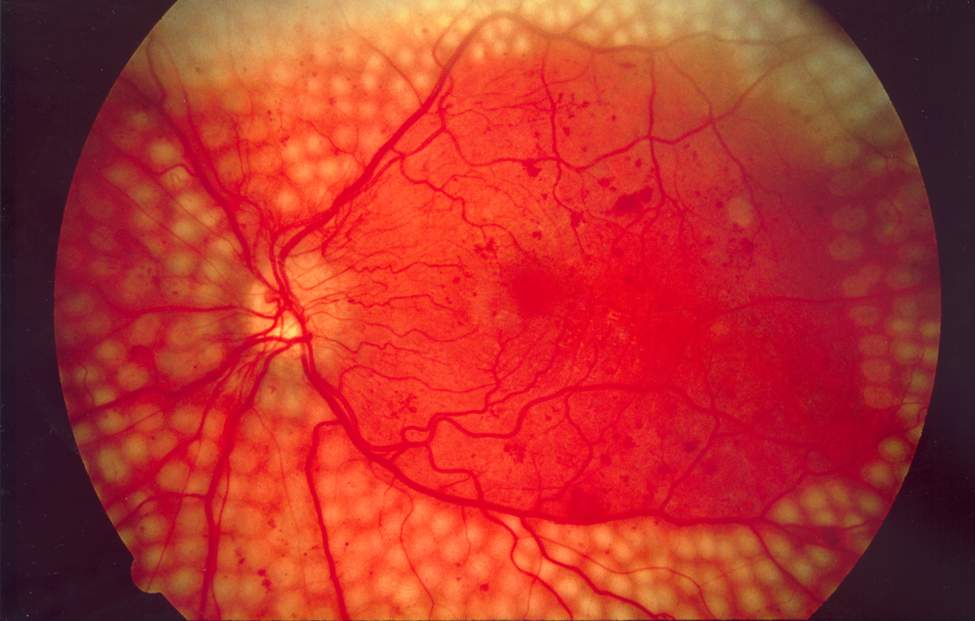
L'origine de la rétinopathie repose sur la toxicité de l'excès de glucose dans le sang, qui provoque une modification progressive de la paroi des vaisseaux rétiniens. L'hyperglycémie chronique fragilise les capillaires, entraînant une rupture de la barrière hémato-rétinienne (interne et externe), des fuites, des hémorragies et, aux stades avancés, la prolifération de néovaisseaux anormaux. La maladie évolue sans symptôme pendant des années, d'où l'importance capitale du dépistage systématique.
À l'échelle mondiale, environ 30 % des patients diabétiques présentent des signes de rétinopathie, et 4,2 millions de personnes souffrent d'une forme menaçant la vision. En France, on estime qu'un patient diabétique sur trois est concerné. Fait préoccupant : 50 % des patients ne sont dépistés qu'à un stade tardif de la maladie, alors qu'un dépistage régulier et un traitement précoce permettent de prévenir la perte de vision dans plus de 90 % des cas.
La prévalence de la rétinopathie diabétique augmente avec la durée du diabète : après 20 ans d'évolution, plus de 80 % des diabétiques de type 1 et 60 % des diabétiques de type 2 présentent une forme de rétinopathie. Le déséquilibre glycémique, l'hypertension artérielle et la dyslipidémie en accélèrent la progression.